Udostępnianie literatury|Strategie i przykłady oczyszczania białek
Streszczenie:
W tym artykule dokonano przeglądu dwóch kluczowych czynników, które należy wziąć pod uwagę w strategiach oczyszczania białek: niższe wymagania dotyczące zastosowania i cechy biologiczne samych białek. Artykuł podkreśla, że wysokiej jakości oczyszczanie białek jest podstawą niezawodności i powtarzalności danych eksperymentalnych, szczególnie dla produkcji rekombinowanych białek. Różne scenariusze zastosowania mają specyficzne wymagania dotyczące czystości białek, aktywności lub zawartości endotoksyny, a charakterystyka białek może znacząco wpłynąć na strategie oczyszczania. Według konkretnych przypadków artykuł pokazuje, że unikalne białka powinny przyjąć niestandardowe schematy oczyszczania. Wreszcie zaproponowano systematyczny proces produkcji białek (ryc. 1), podkreślając kontrolę jakości pełnego procesu od wyboru systemów ekspresji, projekt konstrukcji po optymalizację oczyszczania oraz zalecanie oceny jednorodności białka i funkcjonalności za pomocą technik biofizycznych (takich jak SEC-Mals, DSF itp.). Ten artykuł ma na celu zapewnienie praktycznych wskazówek dla badaczy, pomagając im w sformułowaniu wydajnych i powtarzalnych strategii oczyszczania opartych na cechach i wymaganiach dotyczących zastosowania białek docelowych, zwiększając w ten sposób jakość i wydajność badań naukowych.
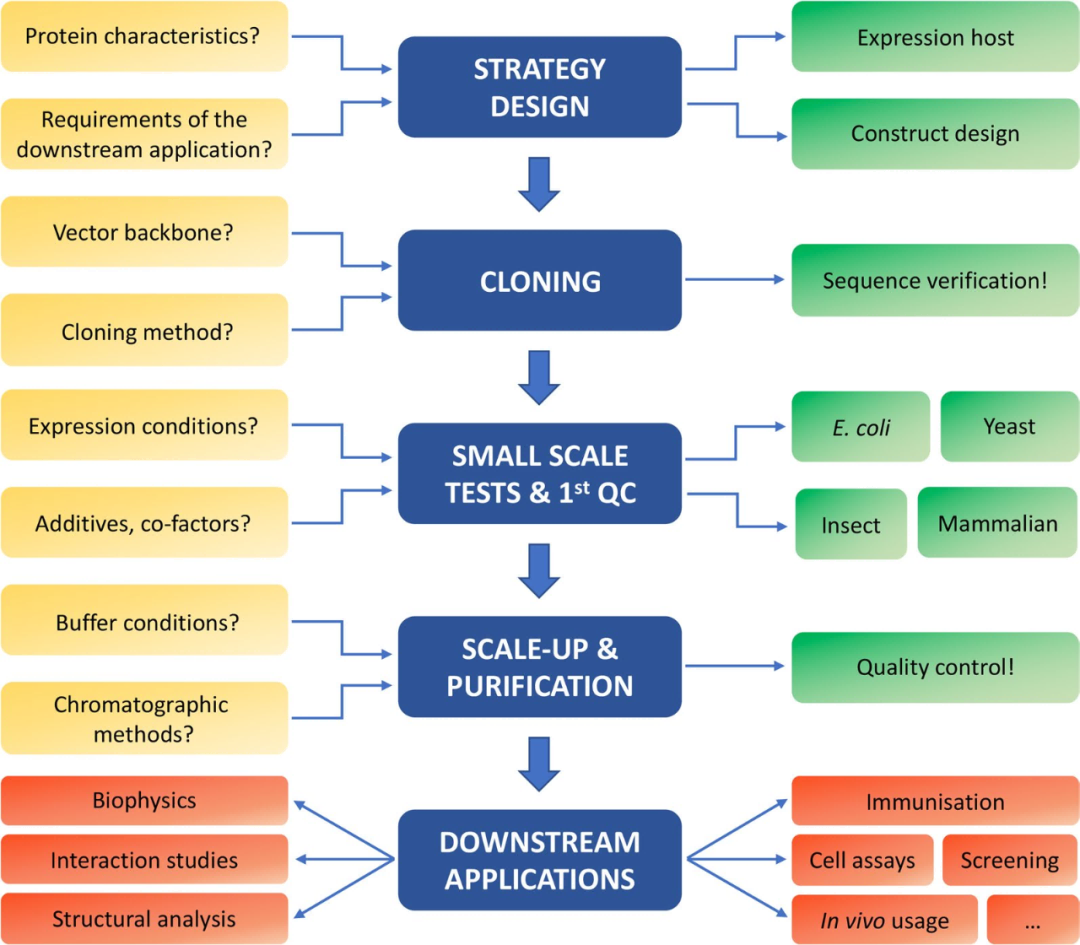
Rycina 1. Schemat procesu produkcji białka
Produkcja białka na wysokim żądanie - przykłady identyfikacji problemu, projektowania strategii łagodzenia i odpowiadającego mu wynikach
1. wiązanie kwasu nukleinowego z białkiem:
Podczas oczyszczania białek wiążących kwas nukleinowy wymagane jest wiele kroków do usunięcia zanieczyszczenia kwasem nukleinowego. Podczas lizy należy dodać nukleazy (takie jak nukleaza SM (benzonaza®) lub DNaza lub RNaza), ale nie można całkowicie usunąć związanych kwasów nukleinowych. Zastąp etapy usuwania kwasu nukleinowego, takie jak wytrącanie siarczanu PEI lub streptomycyna, oczyszczanie heparyny lub chromatografia jonowo-wymiana. Obecność kwasów nukleinowych monitorowano przez stosunek A26 0 nm\/a28 0 nm podczas procesu oczyszczania. Jeśli stosunek był niższy niż 0,6, wskazał, że czystość białka była stosunkowo wysoka, a zanieczyszczenie kwasu nukleinowego było minimalne. W przypadku białek z silnie związanymi kwasami nukleinowymi można je czasowo denaturować (takie jak traktowane mocznikiem), a następnie renaturować. Kluczowe punkty: Użyj wysokiej jakości odczynników, świeżych buforów i czystych kolumn (przed użyciem 0,5 m NaOH).
2. Myszy łańcuch ciężki ferrytyny:
Celem wytworzenia oczyszczonego białka łańcucha ciężkiego mysiego ferrytyny (MFTH1) jest mikroskopia krio-elektronowa o wysokiej rozdzielczości (Cryo-EM). Wektor ekspresyjny Escherichia coli kodowany nieznakowany MFTH1 został zakłócony ultradźwiękowo bez dodawania jakiejkolwiek nukleazy. Po podgrzaniu w stopniu 7 0 poddano on etapom chromatografii chromatografii dializy i wielkości. Powstała próbka wykazała obecność dużej ilości zanieczyszczeń w obrazach mikroskopii krioelektronowej (ryc. 2A), co było całkowicie nieodpowiednie dla jej zastosowania. Zoptymalizuj kroki. Dodaj nukleazę SM podczas procesu lizy komórek i procesu dializy po wytrącaniu siarczanu amonu, a następnie dodaj krok chromatografii wymiany anionów, aby zmniejszyć stosunek A26 0 nm\/a280nm z 1,4 do 0,8. Po wielkości chromatografia wykluczająca stosunek A260NM\/A280 nm końcowej próbki MFTH1 wynosił 0,56. Obrazy mikroskopii SDS-PAGE i krioelektronowej (ryc. 2B) wykazały, że białko było bardzo czyste, co wskazuje, że zanieczyszczenia zostały skutecznie usunięte.
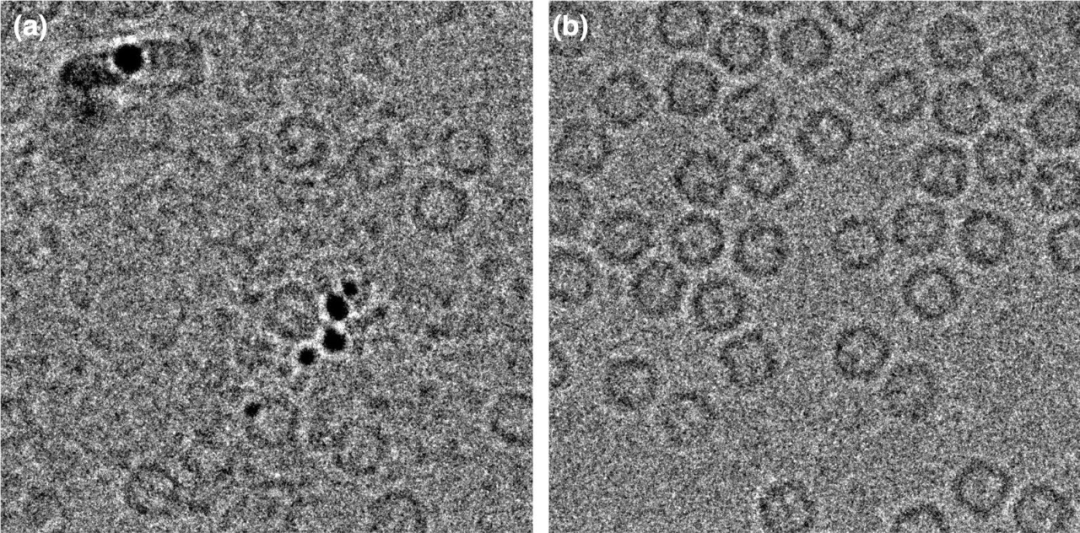
Ryc. 2 Mysie łańcuch ciężki ferrytyny
3. Chimeryczne białko ludzkie DSRBEC (DSRBD-EGF-chimera):
DSRBEC powstaje przez fuzję dwuniciowej domeny wiążącej RNA (DSRBD) ludzkiej kinazy białkowej R i ludzkiego czynnika wzrostu naskórka (HEGF). Gdy DSRBD jest wyrażany w Escherichia coli, wykazuje wyjątkowo wysoką zdolność wiązania dsRNA. Po lizie komórek zanieczyszczający RNA utrudni wiązanie rekombinowanych białek z kolumną stałej chromatografii powinowactwa jonowego (IMAC). Konwencjonalne metody, takie jak wytrążenie siarczanu PEI lub streptomycyna, obróbka RNazy lub roztwory buforowe o wysokiej zawartości soli nie mogą usunąć RNA. Lizę komórek przeprowadzono za pomocą buforu zawierającego 4M mocznik. Supernatant został załadowany do kolumny iMac, a 4M do 0 M mocznik powoli używany przez noc (renaturacja kolumn). Bufor renaturacji dodano z imidazolu i eluowano z kolumny iMac. Ostateczne udoskonalenie przeprowadzono za pomocą filtracji żelowej Superdex 75 w celu uzyskania funkcjonalnie aktywnego DSRBEC.
4. Białka związane z kationami zbieżnymi lub innymi kofaktorami:
W przypadku białek, które wchodzą w interakcje z kationami Bynom, takimi jak Zn 2+, Fe 2+, Cu 2+ lub innymi kofaktorami, kluczowe jest dodanie konkretnych kationów Dyspomentacyjnych (lub innych kofaktorów) podczas wyrażenia. Podczas procesu oczyszczania wymagana jest również niewielka ilość tych samych kationów bilansowych (lub innych kofaktorów). Należy jednak unikać zastosowania wszelkich środków chelatowych (takich jak EDTA, EGTA) i środków redukujących chelating (takich jak DTT lub DTE). Podczas radzenia sobie z białkami związanymi z kationami dwuwartościowymi, należy zastosować mieszaninę inhibitorów proteazy bez środków chelatujących, aby potwierdzić faktyczną obecność kationów dwuwartościowych (lub innych kofaktorów) w oczyszczonym białku za pomocą metod spektroskopowych (takich jak spektrofotometria absorpcji atomowej).
5. Rekombinowana ferridoksyna (RFD) zawierająca pojedynczy klaster [2FE ± 2S] z termofilnego cyjanobakterii mastigocladus laminosus
Ferridoksyna jest rozpuszczalnym białkiem żelaza-siarczkowym, które uczestniczy w reakcjach przenoszenia elektronów. Ferroredoksyna typu roślinnego przenosi pojedynczy klaster [2fe ± 2s] jako akceptor elektronów fotosystemu I. Szczep Escherichia coli BL21 (DE3) wyrażał rekombinowane białko RFD w pożywce TB zawierającej 10 mm FECL3 i antybiotyki. Elucję kolumny przechwytywania IMAC przeprowadzono za pomocą buforu zawierającego 10 mm histydyny, aby uniknąć imidazolu i zapobiec zniszczeniu klastra [2FE ± 2S]. Wymiana anionowa i chromatografia wykluczenia wielkości zastosowano do dalszego oczyszczania i stężenia do 12 mg\/ml do badań przesiewowych. W porównaniu z rekombinowaną produkcją ferroredoksyny, naturalna ferroredoksyna oczyszczona z błękitno-zielonych alg laminosus osiągnęła wyższą rozdzielczość podczas krystalizacji.
6. Białka stosowane jako antygeny
Białka są często stosowane jako antygeny do odzyskiwania ligandów specyficznych dla celu. Pierwszą rzeczą do rozważenia jest to, czy białko jest używane do odporności in vivo w celu uzyskania konwencjonalnego monoklonalnego lub poliklonalnego IgG, czy w programach obejmujących procesy selekcji IgG wielbłąda lub in vitro.
6.1 Antygeny stosowane do rutynowej produkcji przeciwciał
Gdy antygeny są używane do wytwarzania monoklonalnych przeciwciał IgG, prawidłowe fałdowanie antygenu zwykle nie jest konieczne, ponieważ większość przeciwciał monoklonalnych rozpoznaje epitopy liniowe, na które nie mają duży wpływ struktura antygenu, a nawet denaturowane antygeny (takie jak białka ciała). Jednak czystość musi być ściśle kontrolowana, aby uniknąć silnych zanieczyszczeń immunogennych zakłócających odpowiedź immunologiczną i powodować dominację przeciwciał nie-celowych.
6.2 Badanie biblioteki sprzężonej
Szczególną uwagę należy zwrócić na utrzymanie naturalnej konformacji antygenu podczas przetwarzania biblioteki nanobody uzyskanej przez immunizację wielbłąda. W przeciwieństwie do konwencjonalnych przeciwciał, przeciwciała wielbłądów (zwłaszcza nanobodie) zwykle rozpoznają epitopy strukturalne, które są związane z ich unikalną wypukłą komplementarną strukturą miejsca. Podobnie, podczas badania dużych bibliotek przeciwciał syntetycznych lub naturalnych in vitro, antygen musi utrzymać strukturę, która jest całkowicie zgodna z zastosowaniem docelowym. Ponieważ sam proces badań przesiewowych nie jest uprzedzony, jeśli antygen ma nieprawidłowe fałdowanie, agregację lub heterogeniczność konformacyjną, można prześwietlić dużą liczbę koniugatów ukierunkowanych na nienaturalne epitopy.
7. Białka zawierające wiązania międzycząsteczkowe lub wewnątrzcząsteczkowe lub wolną cysteinę
Wiązania disiarczkowe są kluczowe dla stabilizacji naturalnej struktury białek. Podczas procesu oczyszczania, podczas oczyszczania białek zawierających wiązania międzycząsteczkowe lub wewnątrzcząsteczkowe, konieczne jest uniknięcie dodawania czynników redukujących, aby zapobiec zmianom konformacyjnym białek, zmieniając w ten sposób ich funkcje. W przypadku białek zawierających wolną cysteinę środki zmniejszające są niezbędne na wszystkich etapach procesu oczyszczania, szczególnie podczas przechowywania, aby zapobiec tworzeniu sztucznych wiązań disiarczkowych. Najczęściej stosowanymi środkami redukującymi są ditiotreitol (DTT), -mercaptoetanol (-me) i Tris (2- karboksyylo) fosfiny hydrochlorek fosfiny (TCEP). W przypadku żywic IMAC, które są niezgodne z DTT lub TCEP, zaleca się użycie -me i zastąpienie ich innymi środkami redukującymi w kolejnych etapach.
8. Rekombinowane fragment przeciwciał
Chociaż struktura rekombinowanych fragmentów przeciwciał (takich jak nanobodie) jest prostsza niż IgG, ich funkcja zależy od prawidłowego tworzenia wiązań disiarczkowych. W bakteryjnych systemach ekspresji, nawet przy przyjęciu strategii optymalizacji, nadal mogą wystąpić nieprawidłowe lub częściowo złożone produkty, które istnieją zarówno w części rozpuszczalnej, jak i w ciele inkluzyjnym. Bardziej ukryte jest to, że nawet prawidłowo złożone fragmenty przeciwciał mogą tworzyć rozpuszczalne agregaty (agregacja koloidalna) poprzez hydrofobowe płytki na powierzchni. Takie agregaty są trudne do zidentyfikowania w rutynowych testach funkcjonalnych (takich jak ELISA), ponieważ wiązanie wielowartościowe może maskować spadek powinowactwa monomeru, ale ich obecność może poważnie wpływać na zastosowania, które opierają się na wielkości małej cząsteczki (takich jak mikroskopia super rozdzielczości). Dlatego poleganie wyłącznie na SDS-PAGE jest niewystarczające do oceny jakości próbki. Metody biofizyczne, takie jak filtracja żelowa (ryc. 3), należy przyjąć w celu odróżnienia monomerów (głównych pików) od agregatów (piki objętości wykluczenia). Kluczowe punkty kontrolne obejmują: optymalizację środowiska redoks podczas ekspresji w celu promowania tworzenia wiązań disiarczkowych oraz optymalizację warunków przechowywania po oczyszczeniu w celu zapobiegania agregacji. Miary te są kluczowe dla zapewnienia monodyspersyjności i funkcji fragmentów przeciwciał.
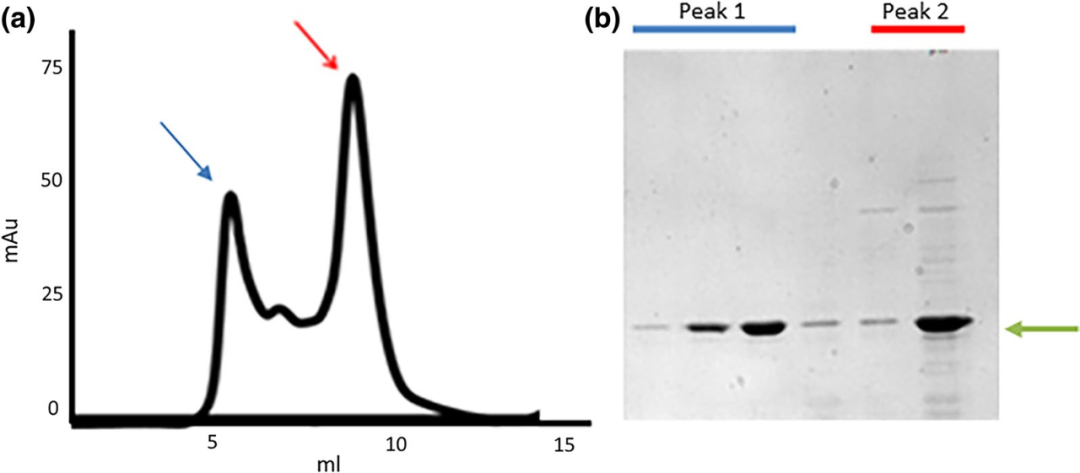
Rycina 3. Oddzielenie filtracji żelowej rozpuszczalnych agregatów nanobodii
9. Rozpuszczalne fragmenty receptora limfocytów LLT1
Rekombinowana ekspresja białek zależnych od wiązania disiarczkowego (takich jak receptor limfocytów LLT1) często staje w obliczu trudności w składaniu. Filtracja żelowa LLT1 typu dzikiego wykazała piki agregacji i pików dimerowych (ryc. 4A), ale spektrometria masowa ujawniła nieprawidłowe fałdowanie spowodowane niesparowaną cysteiną w dimerie (ryc. 4B). W tym celu zaprojektowano dwa mutanty: jeden usunął problem cysteiny, co powoduje nagłe spadek wydajności (ryc. 4A); Po wprowadzeniu neocysteiny do rekonstrukcji zgodnego wiązania disiarczkowego mutant miał nie tylko wysoką wydajność i dobrą stabilność, ale także może krystalizować (ryc. 4C), a struktura 3D potwierdziła, że mutant utworzył prawidłowe wiązanie dwusiarczkowe i utrzymywał naturalne fałdowanie. Przypadek ten pokazuje, że poprzez racjonalne zaprojektowanie konformalnych wiązań disiarczkowych, w połączeniu z filtracją żelową i analizą spektrometrii masowej, można skutecznie rozwiązać problem składania rekombinowanych białek, a białka funkcjonalne ze stabilnymi strukturami i wysoką wydajnością.
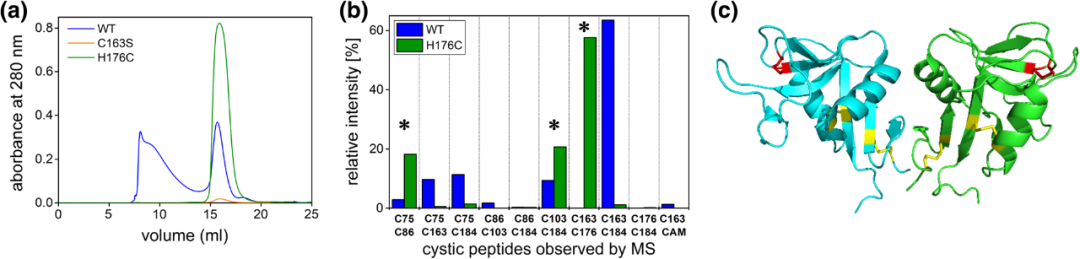
Rycina 4. Rekonstrukcja wiązania disiarczkowego poprawia składanie i wydajność rozpuszczalnego LLT1
10. Łatwo zagregowane białka
Oczyszczanie rekombinowanych białek często stanowi problem agregacji, a jego powstawanie następuje po mechanizmie „wzrostu zarodkowania”-najpierw niewielka ilość rozpuszczalnych agregatów, a następnie wyzwala na dużą skalę nierozpuszczalną agregację. Aby rozwiązać to wyzwanie, należy przyjąć wielopoziomowe strategie: na etapie ekspresji można to osiągnąć poprzez optymalizację szczepu, zmniejszenie temperatury hodowli, wykorzystanie zmodyfikowanych pożywek hodowlanych lub różnych rozpuszczających białek fuzyjnych i zastępowanie systemów ekspresji (komórki owadów\/ssaków) itp. Podczas etapu oczyszczania) jest wymagane, szybkie działanie (w środowisku 4 stopni C), aby uniknąć nadmiernego stężenia białka, a „Strategia komórek oczyszczania”). do SEC) należy przyjąć w celu natychmiastowego usunięcia zagregowanych jąder. Ogólnie rzecz biorąc, podczas roztworów buforowych badań przesiewowych należy wziąć pod uwagę czynniki takie jak skład składowy, wartość pH, czynnik dysocjacyjny lub leubilizator (ryc. 5). Poprzez drobną optymalizację wykrywania ortogonalnego (takiego jak SEC, CD, LS, DSF i przesunięcie temperatury w oparciu o ciepło fluorescencyjne itp.), Określono jakość białka i najbardziej odpowiedni roztwór buforowy.
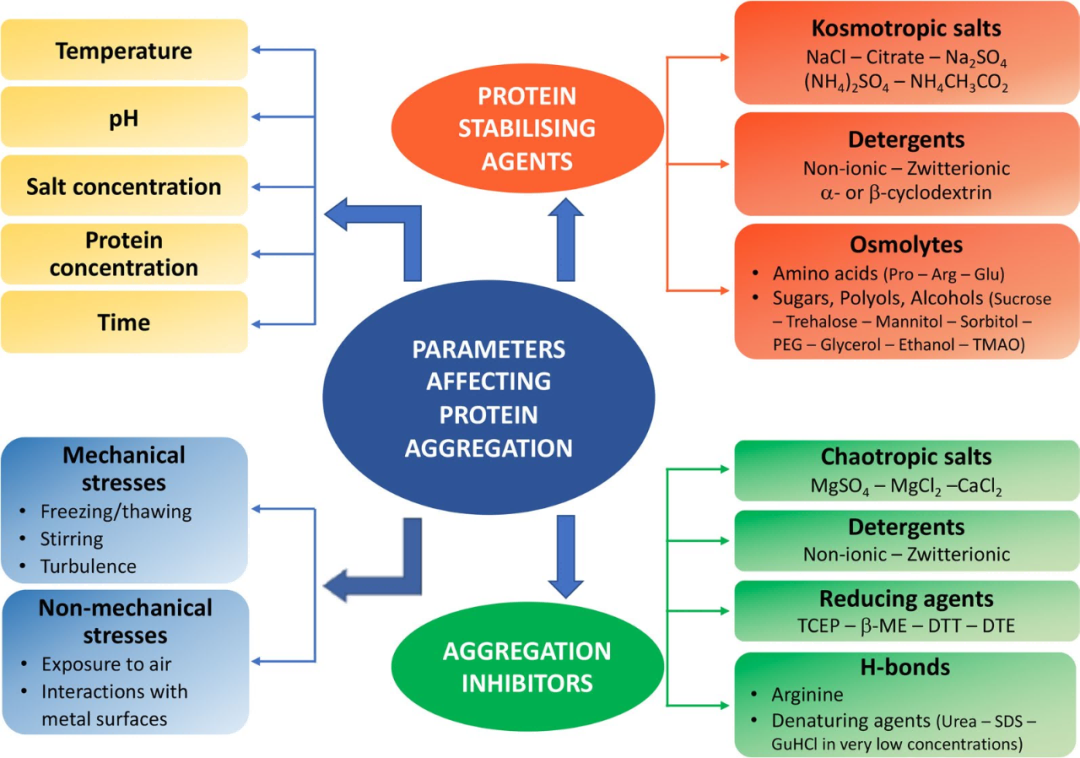
Rycina 5. Strategie łagodzenia agregacji białek
11. Krystalizacja ludzkiej kinazy CLK1 (jak uzyskać powtarzalne partie)
Aby uzyskać jednorodną niefosforylowaną kinazę CLK1 do badań krystalizacji, przyjęto schemat współpracy z wieloma strategią. Po pierwsze, został współekspresja z fosfatazą λ w Escherichia coli w celu wyeliminowania heterogeniczności autofosforylacji. Chociaż wydajność została zmniejszona, zapewniono całkowitą defosforylację. Po schwytaniu przez IMAC eluent uzupełniono stabilizatorami (50 mm argininy, kwas glutaminowy 50 mm i 10 mm DTT), aby zapobiec agregacji, skoncentrowanej, a jego znacznik usunięto przez trawienie TEV. Następnie prawidłowy oligomer oddzielono SEC (zawierającym 5% glicerolu i -me). Ostateczny etap giełdy o kluczowej wymianie anionów rozróżnia krystaliczne (niefosforylowane) i niekrystaliczne (częściowo fosforylowane) grupy CLK1. Warto zauważyć, że tryb lizy komórkowej znacząco wpływa na stabilność białka-metoda wysokociśnieniowa i wysokiej temperatury prowadzi do nieodwracalnej agregacji CLK1, co podkreśla znaczenie łagodnego leczenia przygotowania kinazy.
12. Produkuj galektynę -1 ze stabilną zdolnością wiązania ligandu
Aby przygotować funkcjonalną galektynę -1 dla badań wiązania ligandu, strategie ekspresji i oczyszczania czterech konstruktów (nieobsługiwane i znakowane HIS Galektyna typu dzikiego -1 zostały porównywane. Kluczowe ustalenia wskazują, że oczyszczanie chromatografii powinowactwa w laktozie może skutecznie badać prawidłowo złożone białka, ale należy je połączyć z dokładną dializą (bufor HEPES), aby całkowicie usunąć laktozę z miejsca wiązania i przywrócić aktywność CRD. Galektyna typu dzikiego -1 jest podatna na utlenianie i inaktywację, a jej stabilność pozostaje ograniczona nawet w obecności środków redukujących (ryc. 6). Jednak mutant wolny od cysteiny znacznie zwiększa długoterminową stabilność przy jednoczesnym zachowaniu porównywalnej aktywności aglutynacji i stabilności termicznej (weryfikowanej przez NANODSF, ITC itp.) Poprzez wyeliminowanie uzależnienia od wiązania disiarczkowego.
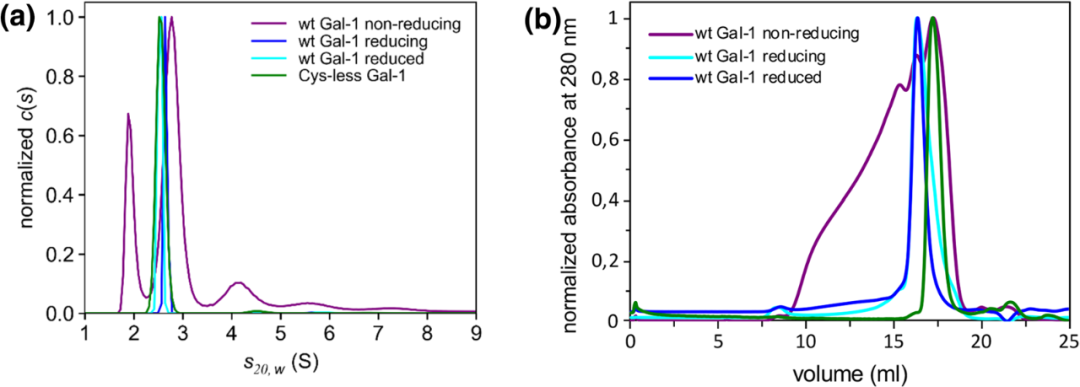
Rycina 6. Charakterystyka hydrodynamiczna rekombinowanej galektyny -1 ujawnia swoją niestabilność
13. Usuwanie endotoksyny
Metoda usuwania endotoksyny oparta jest na chromatografii powinowactwa, w tym w przypadku chromatografii pozytywnie naładowanej (wymiana anionowa), zastosowaniu ligandów polikationowych (takich jak poli-L-lizyna (PLL), unieruchomionej poliaminy (polimyksyny B)) i dodaniu środka surfaktowego Triton X {2}}. Podczas procesu oczyszczania zwróć uwagę na przygotowanie roztworu buforowego z wodą bez LPS i użyj nowych kolumn lub kolumn, które były używane tylko w innych oczyszczaniach wolnych od LPS. W przypadku zanieczyszczenia endotoksyny system pompy chromatograficznej\/płynów można inkubować przez noc w 0. 5m NaOH lub przez 4 godziny w 1. 0 m NaOH. Ostateczną ilość LPS w próbce oceniono za pomocą odczynnika lizatu amebocytów Limulus (LAL) i zweryfikowano, czy był poniżej limitu wymaganego dla konkretnego zastosowania.
14. Kompleks białkowy
Ekspresja i oczyszczanie kompleksów białkowych należy zoptymalizować zgodnie z określonymi warunkami. Wyzwania obejmują niestabilność lub nieprawidłowe fałdowanie podjednostek. Każda podjednostka może być wyrażana niezależnie i montowana in vitro lub koekspresja w celu utworzenia funkcjonalnych kompleksów białkowych. Projekt konstrukcji powinien być starannie wprowadzony z etykietami oczyszczania lub wykrywania, aby uniknąć zakłócania montażu, szczególnie gdy złożone informacje są ograniczone i wymagane są wiele optymalizacji. Podczas procesu oczyszczania integralność i stabilność złożonego należy ocenić. Metody obejmują SDS-PAGE (wykrywanie podjednostki), SEC (jednorodność), SEC-Mals (analiza masy molowej), fotometrię masową lub naturalną spektrometrię mas (weryfikacja masy). Należy zauważyć, że kompleks może dysocjować w niskich stężeniach. W tym czasie należy zoptymalizować metodę lub bufor chromatograficzny (np. Przez warunki przesiewowe dryfu termicznego lub DSF). Ponadto zmniejszenie etapów oczyszczania może zapobiec utratę słabych podjednostek interakcji i zrównoważyć wydajność oczyszczania i integralność kompleksu.
15. Oczyszczanie kompleksów antygen-przeciwciało
Kompleksy przeciwciała-antygenu są typowymi przykładami kompleksów białkowych. Ich korekrystalizacja może ujawnić wzorce wiązania i poprowadzić optymalizację inżynierii przeciwciał. Tradycyjne metody wymagają oddzielnego oczyszczania antygenów i przeciwciał, a następnie ich mieszania. Jednak ostatnie badania wykazały, że strategie koekspresji i współczesności są bardziej wydajne. Potrzebne jest tylko jedno oczyszczenie, aby uzyskać kompleks, a jednocześnie niestabilne antygeny można ustabilizować za pomocą przeciwciał, a nawet ekspresję bez etykiety można osiągnąć. W tej konkretnej sytuacji SDS-PAGE i Filtracja żelowa (SEC) są zwykle wystarczające do oceny czystości i jakości kompleksu.
Streszczenie
Oczyszczanie białka jest fundamentalną technologią w badaniach naukowych. Produkcja białek w skali akademickiej zwykle przestrzega standardowych strategii i może wytwarzać wysokie białka na poziomie miligramu, rozpuszczalne białka, które są szeroko stosowane w biologii strukturalnej, biochemii i badaniach funkcjonalnych. Jednak specjalne wymagania zastosowań niższych (takich jak potrzeba braku endotoksyny w eksperymentach na zwierzętach i zanieczyszczenie nukleaza w badaniach kwasu nukleinowego) lub nieodłączne cechy białek (takich jak łatwa agregacja, zawierające wiązania disarstwowe lub wysokie powinowactwo kwasu nukleinowego) często wymagają niestandardowych roztworów. Przegląd ten, w odpowiedzi na te szczególne okoliczności, proponuje dopracowane strategie od wyboru systemów ekspresyjnych, konstrukcji konstrukcji (optymalizacji etykiet i granic domen) po proces oczyszczania i wprowadza kontrolę jakości (takie jak SEC, SDS-PAGE, wykrywanie aktywności itp.) W kluczowych krokach. Niektóre zastosowania wymagają również dodatkowej analizy (takich jak wykrywanie endotoksyny i określenie reszt kwasu nukleinowego), podobne do koncepcji „zapewnienia jakości” (QA) w branży biofarmaceutycznej, czyli w celu zapobiegania wadom w procesach systematycznych. Opracowując wytyczne dotyczące kontroli jakości i wyjaśnianie określonych standardów odczynników białkowych stosowanych w badaniach naukowych, celem jest ustanowienie bardziej rygorystycznych norm oczyszczania białek dla laboratoriów akademickich, zwiększenie wiarygodności i powtarzalności danych eksperymentalnych oraz wypełnienie luki między podstawowymi badaniami i standardami przemysłowymi.
Doi: 10.1186\/s 12934-022-01778-5

